Che cosa è iltensione superficiale dell'acqua?
Tensione superficialeè la tendenza delle superfici di appoggio liquide a restringersi fino a raggiungere la minima area superficiale possibile. La tensione superficiale consente agli oggetti con una densità maggiore dell'acqua, come lamette da barba e insetti (ad esempio, water striders), di galleggiare su una superficie d'acqua senza nemmeno immergersi parzialmente.
Nelle interfacce liquido-aria, la tensione superficiale è dovuta alla maggiore attrazione delle molecole del liquido tra loro (dovuta alla coesione) rispetto alle molecole dell'aria (dovuta all'adesione).
Ci sono due meccanismi primari in gioco. Uno è una forza verso l'interno sulle molecole di superficie che causa la contrazione del liquido. Il secondo è una forza tangenziale parallela alla superficie del liquido. Questotangenzialela forza è generalmente definita tensione superficiale. L'effetto netto è che il liquido si comporta come se la sua superficie fosse ricoperta da una membrana elastica allungata. Ma questa analogia non deve essere portata troppo oltre poiché la tensione in una membrana elastica dipende dalla quantità di deformazione della membrana mentre la tensione superficiale è una proprietà intrinseca del liquido–aria oliquido-vaporeinterfaccia.
A causa dell'attrazione relativamente elevata delle molecole d'acqua tra loro attraverso una rete di legami idrogeno, l'acqua ha una tensione superficiale più elevata (72,8 millinewton (mN) per metro a 20 gradi) rispetto alla maggior parte degli altri liquidi. La tensione superficiale è un fattore importante nel fenomeno della capillarità.
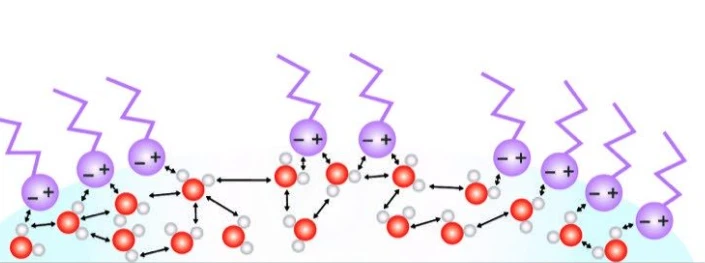
Perché il sapone interrompe la tensione superficiale dell'acqua?
Il sapone rompe la tensione superficiale dell'acqua grazie alla sua struttura molecolare, che contiene sia estremità idrofobiche (che respingono l'acqua) sia idrofile (che attraggono l'acqua). Le molecole d'acqua in superficie creano una "pelle" grazie alle forze coesive tra loro, portando a un'elevata tensione superficiale.
Quando il sapone viene aggiunto all'acqua, le estremità idrofobiche delle molecole di sapone vengono respinte dall'acqua e si fanno strada verso la superficie, mentre le estremità idrofile rimangono nell'acqua. Ciò interrompe le forze coesive tra le molecole d'acqua in superficie, riducendo la tensione superficiale. Di conseguenza, l'acqua diventa meno coesiva e si diffonde più facilmente, consentendole di bagnare meglio le superfici.





